
编者按:直接从胰腺癌研究者Kirsten Bryant博士和胰腺癌行动网络的总裁兼首席执行官Julie Fleshman那里听到CBSN采访于2019年3月4日进行。
一个意想不到的实验室发现指出了一种新的联合治疗策略胰腺癌的两项研究发表在自然医学今天。
论文-一项研究主要来自北卡罗莱纳大学的Lineberger综合癌症中心另一个来自犹他大学亨茨曼癌症研究所的研究——看看使用药物的目标激活的蛋白质克拉斯与一种阻断自噬过程的药物结合。
KRAS是最常见的突变蛋白胰腺肿瘤它被冠以“不可用药”的恶名,因为之前直接对其进行治疗的努力都没有成功。因此,研究人员试图关闭突变KRAS激活的部分——作为停止KRAS活动本身的替代品。
但是,研究人员很快发现,被KRAS激活的阻断蛋白不足以阻止胰腺癌细胞的生长。

Channing Der博士(最左)和Adrienne Cox博士(最右)的实验室小组。
克里斯汀•布莱恩特,博士,论文第一作者,来自Lineberger癌症中心小组,加入著名KRAS专家实验室钱宁Der博士2013年作为博士后研究员。科比和德尔都获得了胰腺癌行动网该基金对这项新发表的研究做出了贡献。
科比的主要兴趣是胰腺癌的新陈代谢,也就是癌细胞收集和利用营养的过程与健康细胞不同。虽然最初对KRAS和新陈代谢之间的关系持怀疑态度,但Der给了Bryant一个机会去追求她的科学兴趣。
“自噬是胰腺癌细胞进行新陈代谢的一种不同寻常的方式;这些细胞基本上开始吞噬自己,”布莱恩特解释道。“这种自我进食让细胞从自身的内部成分中获得重要的营养。”
突变KRAS产生的蛋白信号与自噬之间的联系尚不清楚。然而,Bryant回忆道,她假设阻断KRAS也会阻止细胞参与自噬——因为胰腺癌细胞内发生的许多过程都是由突变KRAS直接或间接协调的。
她说:“我们惊讶地发现相反的结果是正确的——当KRAS信号被关闭时,自噬变得更强。”
另一个惊喜是科比和德。
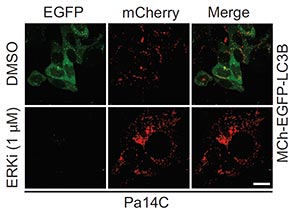
出乎意料的是,在胰腺癌细胞中阻断突变KRAS信号导致自噬增加,如ERKi行中红色染色增加和绿色染色减少所示。
Bryant说:“在2017年12月的一次会议上,我展示了抑制ERK (KRAS激活的一种蛋白质)的结果,并发现自噬增加。”她回忆起一位同事,马丁·麦克马洪博士,对她的海报演讲表现出极大的兴趣。
几天后,McMahon给Der发邮件解释说,他的研究小组也有了类似的发现——只不过他们的研究重点是KRAS信号通路中的一种名为MEK的蛋白质,而不是ERK。
布莱恩特说:“我们决定定期见面,然后共同提交我们的手稿,而不是先看谁发表文章。”
“这些文件放在一起会更牢固。”
当看到一个独立的研究团队复制了与他们相似的研究成果时,Bryant感到深深的认可,他还惊讶地发现,McMahon实验室的医学博士、博士后、肿瘤专家柯南·金赛(Conan Kinsey)曾用提出的联合疗法治疗过一位患者。
虽然他已经去世了,但这位病人经历了5个多月的无进展生存,在此之前,他似乎已经精疲力竭了治疗方案提供给他。

在PanCAN的全国胰腺癌宣传日上,Bryant举着她父亲在国会大厦前的照片。
这是科比个人的斗争,他失去了父亲在2013年被诊断为胰腺癌的11个月后。
“当我想到柯南治疗的病人时,我就想起了我的父亲,”布莱恩特说。“他也别无选择,而我的研究我不能再帮助他了,想到我正在做的工作可以帮助别人,我心里充满了保护的自豪感。”
布莱恩特补充说,“我把我父亲的名字放在论文的致谢部分,通常保留给资助来源和支持科学或论文准备的个人。
“感谢他‘持续的灵感’。”
至于下一步,Bryant说她正在寻找其他方法来阻止KRAS的信号传递,并努力寻找更有效的策略来抑制自噬。而且,德尔和麦克马洪的团队都在建立临床试验正式测试联合治疗方法,确定其在胰腺癌患者中的安全性和有效性。
科比说:“我为自己正在做的事情感到骄傲,如果没有PanCAN,这一切都不可能实现。”

 877-272-6226
877-272-6226









